Kyselina dusičná (HNO 3), bezfarebná, dymivá a vysoko leptavá kvapalina (bod tuhnutia -42 ° C [-44 ° F], bod varu 83 ° C [181 ° F]), čo je bežné laboratórne činidlo a dôležité priemyselná chemikália na výrobu hnojív a výbušnín. Je toxický a môže spôsobiť vážne popáleniny.
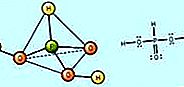
oxykyselina: Kyselina dusičná a dusičnany
Kyselina dusičná, HNO3, bola známa alchymistom 8. storočia ako „aqua fortis“ (silná voda). Je tvorená
Príprava a použitie kyseliny dusičnej boli známe raným alchymistom. Bežný laboratórny postup používaný mnoho rokov, ktorý pripisoval nemecký chemik, Johann Rudolf Glauber (1648), spočíval v zahrievaní dusičnanu draselného koncentrovanou kyselinou sírovou. V roku 1776 Antoine-Laurent Lavoisier ukázal, že obsahuje kyslík, av roku 1816 Joseph-Louis Gay-Lussac a Claude-Louis Berthollet založili svoje chemické zloženie.
Hlavnou metódou výroby kyseliny dusičnej je katalytická oxidácia amoniaku. Pri metóde vyvinutej nemeckým chemikom Wilhelmom Ostwaldom v roku 1901 sa plynný amoniak postupne oxiduje na oxid dusnatý a oxid dusičitý vzduchom alebo kyslíkom v prítomnosti katalyzátora na báze platiny. Oxid dusičitý sa absorbuje vo vode za vzniku kyseliny dusičnej. Výsledný roztok kyseliny vo vode (asi 50 - 70% hmotnostných kyseliny) sa môže dehydratovať destiláciou kyselinou sírovou.
Kyselina dusičná sa rozkladá na vodu, oxid dusičitý a kyslík a vytvára nahnedlý žltý roztok. Jedná sa o silné kyseliny, úplne ionizovanej do hydronium (H 3 O +) a dusičnan (NO 3 -) ióny vo vodnom roztoku, a silné oxidačné činidlo, (ten, ktorý sa chová ako akceptor elektrónov v oxidačno-redukčných). Medzi mnoho dôležitých reakcií kyseliny dusičnej patrí: neutralizácia amoniakom za vzniku dusičnanu amónneho, hlavnej zložky hnojív; nitráciu glycerolu a toluénu, tvoriacu výbušniny nitroglycerín a trinitrotoluén (TNT); príprava nitrocelulózy; a oxidácia kovov na zodpovedajúce oxidy alebo dusičnany.