Borán, akákoľvek homológna séria anorganických zlúčenín bóru a vodíka alebo ich derivátov.
chemické viazanie: Boranes
Ako už bolo uvedené vyššie, zlúčenina diboránu s nedostatkom elektrónov, B2H6, sa môže považovať za zhluk atómov držaných pohromade
Hydridy bóru boli prvýkrát systematicky syntetizované a charakterizované v rokoch 1912 až 1937 nemeckým chemikom Alfredom Stockom. Analogicky ich nazýval bórany (nasýtené uhľovodíky), hydridy uhlíka (C), ktoré sú v periodickej tabuľke susedom bóru. Pretože ľahšie borány boli prchavé, citlivé na vzduch a vlhkosť a toxické, Stock vyvinul metódy a prístroje na ich vákuum. Americké práce na bóranoch sa začali v roku 1931, vykonávali Hermann I. Schlesinger a Anton B. Burg. Boranes zostal primárne akademickým záujmom až do druhej svetovej vojny, keď vláda USA podporovala výskum zameraný na nájdenie prchavých zlúčenín uránu (borohydridy) na separáciu izotopov a do 50. rokov 20. storočia, keď podporovala programy na vývoj vysokoenergetických palív pre rakety a prúdové lietadlá. (Borány a ich deriváty majú oveľa vyššie teploty spaľovania ako uhľovodíkové palivá.) William Nunn Lipscomb, Jr., získal Nobelovu cenu za chémiu z roku 1976 „za svoje štúdie o štruktúre bórov osvetľujúce problémy chemickej väzby“, zatiaľ čo jeden zo Schlesingerových študenti, Herbert Charles Brown, zdieľali cenu 1979 za jeho hydroboračnú reakciu (1956), čo je pozoruhodne ľahké pridanie BH3 (vo forme BH 3 · S) na nenasýtených organických zlúčenín (tj, alkény a alkíny) v éteri rozpúšťadla (S), pri teplote miestnosti, čím sa získa organoborany kvantitatívne (ktorá je v reakcii, ktorá prebieha úplne, alebo takmer úplne, do konca). Hydroboračná reakcia zase otvorila nové možnosti výskumu v oblasti stereošpecifickej organickej syntézy.
Tieto Boran, ktoré boli pripravené podľa populácie mala všeobecný zloženie B n H n + 4 a B n H n + 6, ale zložitejšie druhov, a to ako neutrálne a negatívne (aniónové), sú známe. Hydridy bóru sú početnejšie ako hydridy akýchkoľvek iných prvkov okrem uhlíka. Najjednoduchšie izolovateľné boran je B 2 H 6, diborán (6). (Arabská číslica v zátvorkách označuje počet atómov vodíka.) Je to jeden z najviac študovaných a synteticky najužitočnejších medziproduktov. Je komerčne dostupná a roky sa z nej pripravilo veľa boránov a ich derivátov, buď priamo alebo nepriamo. Voľný BH 3 (A a B 3 H 7), sú veľmi nestabilné, ale môžu byť izolované ako stabilné adukty (adičnej produkty) s Lewisovým bázami (elektrón-donorové molekuly) -eg, BH 3 · N (CH 3) 3. Borány môžu byť pevné látky, kvapaliny alebo plyny; ich teploty topenia a teploty varu sa zväčšujú so zvyšujúcou sa zložitosťou a molekulovou hmotnosťou.
Štruktúra a väzba boránov
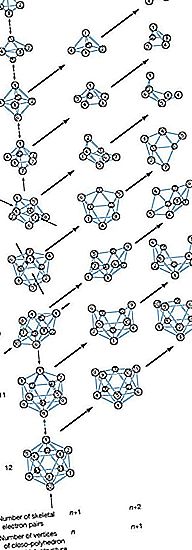
Namiesto toho, aby vykazovali jednoduchú reťazovú a kruhovú konfiguráciu zlúčenín uhlíka, sú atómy bóru v komplexnejších boránoch umiestnené v rohoch polyhedrónov, ktoré sa môžu považovať buď za deltahedróny (polyhedróny s trojuholníkovými plochami) alebo deltaedrické fragmenty. Rozvíjanie porozumenia týchto klastrov bóru pomohlo chemikom racionalizovať chémiu iných klastrových zlúčenín anorganických, organokovových a prechodných kovov.
Jeden z niekoľkých nomenklatúrnych systémov navrhovaných Medzinárodnou úniou čistej a aplikovanej chémie (IUPAC) využíva charakteristické štrukturálne predpony: (1) closo- (korupcia „clovo“ z latinských clovis, čo znamená „klietka“), deltahedrony n atómy bóru; (2) nido- (z latinského nidusu, čo znamená „hniezdo“), neuzatvorené štruktúry, v ktorých klaster B n zaujíma n rohy polyhedronu so štruktúrou (n + 1) - tj kloso-polyhedron s jedným chýbajúcim vrcholom; (3) arachno- (gréčtina, čo znamená „pavučinu“), zhluky, ktoré sú ešte viac otvorené, pričom atómy bóru zaberajú n priľahlé rohy polyhedronu s n (2) hranicami, tj kloso-polyhedrón s dvoma chýbajúcimi vrcholmi; (4) hypho- (gréčtina, čo znamená „tkať“ alebo „sieť“), najotvorenejšie zhluky, s atómami bóru, ktoré zaberajú n rohoch (n + 3) kloso-polyhedronu; a (5) klado- (grécky, čo znamená „vetva“), n vrcholy n + 4-vrcholu kloso-polyhedrónu obsadeného n atómami bóru. Členovia hypo- a klado-série sú v súčasnosti známe iba ako deriváty bóru. Prepojenie medzi dvoma alebo viacerými z týchto polyhedrálnych boranových zhlukov je označené predponou spojovka (latinčina, čo znamená „spojiť sa“). Napríklad conjuncto-B 10 H 16 sa vyrába spojením na B 3 H 8 jednotiek z dvoch B 6 H 9 molekúl B-B väzbou.
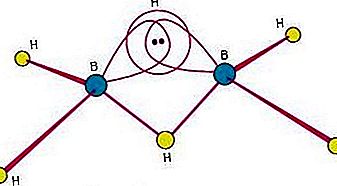
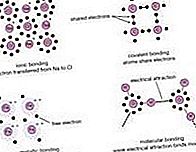
Jedným z dôvodov veľkého záujmu o borány je skutočnosť, že majú štruktúry odlišné od akejkoľvek inej triedy zlúčenín. Pretože väzba v bóranoch zahŕňa multicentrické viazanie, v ktorom tri alebo viac atómov zdieľajú pár väzbových elektrónov, sú borány bežne nazývané elektrón-deficientné látky. Diborane (6) má túto štruktúru:
Táto štruktúra zahŕňa trojväzbovú mostíkovú väzbu, v ktorej je jeden pár elektrónov zdieľaný medzi tromi (skôr ako dvoma) atómami - dvoma atómami bóru a jedným atómom vodíka. (Pozri chemickú väzbu: Pokročilé aspekty chemickej väzby: Borány pre diskusiu o trojväzbovej väzbe.) Schopnosť bóru vytvárať takéto väzby popri bežných kovalentných väzbách vedie k tvorbe komplexných viacstenných bóranov.