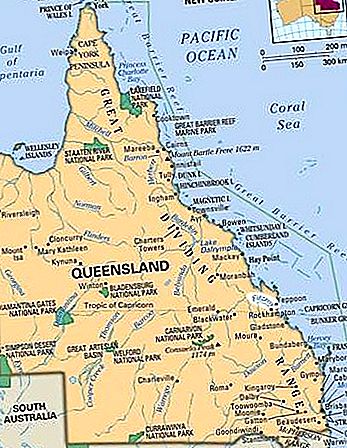
výpotok
Pri výpočte tlaku plynu zvážte vyššie opísaný systém, ale oblasť A v stene nádrže sa nahradí malým otvorom. Počet molekúl, ktoré unikajú otvorom v čase t, sa rovná (1/2) (N / V) v z (At). V tomto prípade sú kolízie medzi molekulami významné a výsledok platí iba pre malé diery vo veľmi tenkých stenách (v porovnaní so strednou voľnou cestou), takže molekula, ktorá sa blíži pri diere, prejde bez zrážky s inou molekulou a odklonenie preč. Vzťah medzi v z a priemernou rýchlosťou v̄ je pomerne jednoduchý: v z = (1/2) v̄.
Ak sa porovnajú rýchlosti pre dva rôzne plyny vytekajúce cez tú istú dieru, počnúc rovnakou hustotou plynu, zistí sa, že oveľa viac ľahkého plynu uniká ako ťažký plyn a že viac plynu uniká pri vysokej teplote ako pri nízkej teplote, ostatné veci sú rovnaké. Najmä
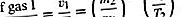
Posledným krokom Z energetického vzorca, (1/2) mv 2 = (3/2) kT, kde (v 2) 1/2 je aproximované byť v, aj keď v 2 a (V) 2 v skutočnosti sa líšia číselný faktor blízko jednoty (konkrétne 3π / 8). Tento výsledok bol experimentálne objavený v roku 1846 Grahamom pre prípad konštantnej teploty a je známy ako Grahamov zákon vytekania. Môže sa použiť na meranie molekulových hmotností, na meranie tlaku pár materiálu s nízkym tlakom pár alebo na výpočet rýchlosti odparovania molekúl z povrchu kvapaliny alebo tuhej látky.
Tepelná transpirácia
Predpokladajme, že dva zásobníky toho istého plynu, ale pri rôznych teplotách, sú spojené malou dierou a že plyn je uvedený do ustáleného stavu. Ak je otvor dostatočne malý a hustota plynu je dostatočne nízka na to, aby došlo len k výtoku, rovnovážny tlak bude vyšší na strane vysokej teploty. Ak sú však počiatočné tlaky na oboch stranách rovnaké, plyn bude prúdiť zo strany s nízkou teplotou na stranu s vysokou teplotou, čo spôsobí zvýšenie tlaku pri vysokej teplote. Posledne menovaná situácia sa nazýva tepelná transpirácia a výsledok v ustálenom stave sa nazýva rozdiel v termomolekulárnom tlaku. Tieto výsledky vyplývajú jednoducho z efúzneho vzorca, ak sa na nahradenie N / V za p / T použije zákon o ideálnom plyne;
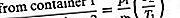
Po dosiahnutí ustáleného stavu sú rýchlosti výtoku rovnaké, a teda
Tento jav prvýkrát experimentálne skúmal Osborne Reynolds v roku 1879 v Manchestri, Eng. Chyby sa môžu vyskytnúť, ak sa tlak plynu meria v nádobe pri veľmi nízkej alebo veľmi vysokej teplote jej pripojením cez jemnú trubicu k manometru pri izbovej teplote. Kontinuálnu cirkuláciu plynu je možné dosiahnuť spojením týchto dvoch zásobníkov s ďalšou rúrkou, ktorej priemer je v porovnaní so strednou voľnou dráhou veľký. Tlakový rozdiel vedie plyn cez túto trubicu viskóznym prúdením. Tepelný motor založený na tomto obehovom prúde má nanešťastie nízku účinnosť.








![Americká história obliehania Waco [1993] Americká história obliehania Waco [1993]](https://images.thetopknowledge.com/img/world-history/5/waco-siege-american-history-1993.jpg)