Sulfid, tiež hláskoval sulfid, niektorý z troch tried chemických zlúčenín, ktoré obsahujú prvok síru. Medzi tri triedy sulfidov patria anorganické sulfidy, organické sulfidy (niekedy nazývané tioétery) a sulfidy fosfínu. Anorganické sulfidy sú iónové zlúčeniny obsahujúce záporne nabitý sulfidový ión, S2-; tieto zlúčeniny sa môžu považovať za soli veľmi slabého kyslého sírovodíka. Organické sulfidy sú zlúčeniny, v ktorých je atóm síry kovalentne viazaný na dve organické skupiny. Fosfínsulfidy sa tvoria reakciou organických fosfínov so sírou, v ktorej je atóm síry spojený s fosforom väzbou, ktorá má kovalentné aj iónové vlastnosti.

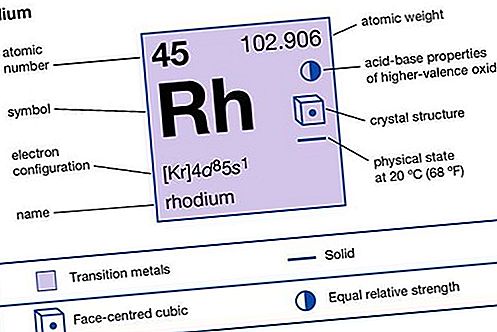
Sulfidy mnohých dôležitých kovových prvkov sú prírodne sa vyskytujúce minerály. Napríklad, pyrit, ktorý je tiež nazývaný Bláznovo zlato vzhľadom k jeho mosadzné žltej farby, je sulfid železa so vzorcom FeS 2. Pyrit je hlavným zdrojom železa a je jedným z najhojnejších minerálov síry. Zinok, kadmium, ortuť, meď, striebro a mnoho ďalších prvkov sa vyskytuje v prírode ako sulfidy.
Príprava sulfidov
Väčšina kovov reaguje priamo so sírou za vzniku sulfidov kovov - tj zlúčenín, ktoré obsahujú atóm kovu a sulfidový ión, S2-. Okrem priamej kombináciu prvkov, ako spôsobu prípravy sulfidy, môžu byť tiež produkované redukciou síranu uhlíkom alebo vyzrážaním z kyslého vodného roztoku sírovodíka, H 2 S, alebo zo základného roztoku sulfidu amónneho, (NH 4) 2 S. Ďalší spôsob, vhodný najmä pre vo vode rozpustné sulfidy, zahŕňa prebublávania H 2 s na základnej roztokom kovu, čím sa získa kovový sírovodík, MHS. Ďalší ekvivalent pridaného hydroxidu kovu poskytne sulfid kovu. NaOH + H 2 S → NaHS + H 2 O
NaHS + NaOH → Na 2 + H 2 O
Rozpustnosť sulfidov
Alkalické kovy a kovy alkalických zemín sú jediné sulfidy, ktoré majú akúkoľvek značnú rozpustnosť vo vode a ktoré sa zdajú byť primárne iónové. Na rozdiel od toho sú sulfidy medi medi a zinku niektoré z najmenej známych známych zlúčenín. Keď sa vo vode rozpustné sulfidy kovov zahrievajú vo vodnom roztoku s elementárnou sírou, tvoria sa takzvané polysulfidy. Tieto riešenia sa skladajú predovšetkým z S 4, 2 a S 3 2- anióny. Sulfidy sú dôležitou súčasťou zdrojov energie s vysokou hustotou, ako sú lítiové a sulfidové batérie. Sulfidy, ktoré sú používané v týchto energetických zdrojov je M 2 S, M 2 S 2, M 2 S 4, a M 2 S 5.