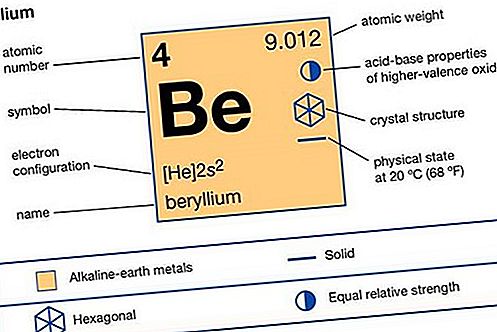
Berylium (Be), predtým (do roku 1957) glucinium, chemický prvok, najľahší člen kovov alkalických zemín skupiny 2 (IIa) periodickej tabuľky, používaný v metalurgii ako tvrdidlo a pri mnohých vesmírnych a jadrových aplikáciách,

kov alkalických zemín
Prvkami sú berýlium (Be), horčík (Mg), vápnik (Ca), stroncium (Sr), bárium (Ba) a rádium (Ra).
Vlastnosti prvku
| atómové číslo | 4 |
|---|---|
| atómová hmotnosť | 9,0122 |
| bod topenia | 1 287 ° C (2 349 ° F) |
| bod varu | 2 471 ° C (4 480 ° F) |
| merná hmotnosť | 1,85 pri 20 ° C (68 ° F) |
| oxidačný stav | +2 |
| elektrónová konfigurácia | 1s 2 2s 2 |
Výskyt, vlastnosti a použitie
Berýlium je kovovo šedý kov, ktorý je pri izbovej teplote pomerne krehký a jeho chemické vlastnosti sa trochu podobajú vlastnostiam hliníka. Vyskytuje sa bezplatne v prírode. Berýlium sa nachádza v beryli a smaragdoch, mineráloch, ktoré boli známe starovekým Egypťanom. Aj keď už dlho existovalo podozrenie, že tieto dva minerály boli podobné, chemické potvrdenie o tom došlo až koncom 18. storočia. Emerald je teraz známy ako zelená odroda berylu. Berylium objavil (1798) ako oxid francúzsky chemik Nicolas-Louis Vauquelin v beryli a smaragdoch a bol izolovaný (1828) ako kov nezávisle nemeckým chemikom Friedrichom Wöhlerom a francúzskym chemikom Antoine AB Bussy redukciou jeho chloridu draslíkom, Berýlium je široko distribuované v zemskej kôre a odhaduje sa, že sa vyskytuje v zemských horninách v rozsahu 0,0002 percenta. Jeho kozmická hojnosť je 20 na stupnici, v ktorej je kremík, štandard, 1 000 000. USA majú asi 60 percent svetového berýlia a sú zďaleka najväčším producentom berýlia; k ďalším významným producentským krajinám patrí Čína, Mozambik a Brazília.
Existuje asi 30 minerálov, ktoré obsahujú berylium, vrátane berylu (Al 2 Be 3 Si 6 O 18, kremičitan berylia hlinitý), bertrandit (Be 4 Si 2 O 7 (OH) 2, kremičitan berylia), fenakit (Be 2 SiO) 4), a chryzoberyl (Beal 2 O 4). (Vzácne formy berylu, smaragdu a akvamarínu majú zloženie, ktoré sa blíži uvedenému zloženiu, ale priemyselné rudy obsahujú menej berýlia; väčšina berylu sa získava ako vedľajší produkt iných ťažobných operácií, pričom väčšie kryštály sa zbierajú ručne..) Zistilo sa, že beryl a bertrandit sú v dostatočnom množstve na vytvorenie komerčných rúd, z ktorých sa priemyselne vyrába hydroxid berylia alebo oxid berylia. Extrakcia berýlia je komplikovaná skutočnosťou, že berýlium je vo väčšine rúd menej významnou zložkou (5 hmotnostných percent dokonca v čistom berýli, menej ako 1 hmotnostné percento v bertrandite) a je pevne viazané na kyslík. Na koncentrovanie berýlia vo forme jeho hydroxidu sa všetky používajú kyseliny, praženie komplexnými fluoridmi a extrakcia kvapalina-kvapalina. Hydroxid sa prevedie na fluorid pomocou fluoridu amónneho berýlia a potom sa zahrieva horčíkom za vzniku elementárneho berýlia. Alternatívne môže byť hydroxid zahrievaný za vzniku oxidu, ktorý môže byť ďalej spracovaný s uhlíkom a chlórom za vzniku chloridu berýlia; Na výrobu kovu sa potom použije elektrolýza roztaveného chloridu. Prvok sa čistí vákuovým tavením.
Berýlium je jediný stabilný ľahký kov s relatívne vysokou teplotou topenia. Aj keď je ľahko napadnutý zásadami a neoxidujúcimi kyselinami, berýlium rýchlo vytvára priľnavý oxidový povrchový film, ktorý za normálnych podmienok chráni kov pred ďalšou oxidáciou vzduchu. Tieto chemické vlastnosti, spolu s vynikajúcou elektrickou vodivosťou, vysokou tepelnou kapacitou a vodivosťou, dobrými mechanickými vlastnosťami pri zvýšených teplotách a veľmi vysokým modulom pružnosti (o tretinu väčšou ako oceľ), ho robia cenným pre štrukturálne a tepelné aplikácie. Vďaka rozmerovej stabilite Beryllium a vysokej schopnosti dosiahnuť vysoký lesk sa stal užitočným pre zrkadlá a uzávery kamier v kozmických, vojenských a lekárskych aplikáciách a pri výrobe polovodičov. Kvôli svojej nízkej atómovej hmotnosti berylium prenáša röntgenové lúče 17-krát rovnako ako hliník a vo veľkej miere sa používa pri výrobe okien pre röntgenové trubice. Berylium sa vyrába do gyroskopov, akcelerometrov a počítačových častí pre inerciálne navádzacie prístroje a iné zariadenia pre riadené strely, lietadlá a vesmírne vozidlá a používa sa pre ťažké brzdové bubny a podobné aplikácie, v ktorých je dôležitý dobrý chladič. Jeho schopnosť spomaliť rýchle neutróny našla značné uplatnenie v jadrových reaktoroch.
Veľa berýlia sa používa ako nízkopercentná zložka tvrdých zliatin, najmä s meďou ako hlavnou zložkou, ale tiež so zliatinami na báze niklu a železa, pre výrobky, ako sú pružiny. Berylium-meď (2% berylia) sa vyrába na náradie, ktoré sa môže použiť v prípade iskrenia, ako je to v práškových továrňach. Samotný berýlium neznižuje iskrenie, ale zosilňuje meď (faktorom 6), ktorá pri náraze nevytvára iskry. Malé množstvá berýlia pridávané k oxidovateľným kovom vytvárajú ochranné povrchové filmy, znižujú horľavosť horčíka a zvyšujú lesk v zliatinách striebra.
Neutróny (1932) objavil britský fyzik Sir James Chadwick ako častice vyvrhnuté z berýlia bombardované alfa časticami zo zdroja rádia. Odvtedy sa ako zdroj neutrónov používa berylium zmiešané s alfa žiaričom, ako je rádium, plutónium alebo americium. Alfa častice uvoľnené rádioaktívnym rozpadom rádia atómov reagujú s atómami berýlia, čím sa získa, medzi produktmi, neutróny s širokú škálu energie, až do asi 5 x 10 6 elektrónvoltov (eV). Ak je však rádium zapuzdrené, takže žiadna z častíc alfa nedosiahne berylium, neutrónovou energiou nižšou ako 600 000 eV sa vytvára viac prenikajúcim gama žiarením z rozpadových produktov rádia. Medzi historicky významné príklady použitia zdrojov berylia / rádia neutrónov patrí bombardovanie uránu nemeckými chemikmi Ottom Hahnom a Fritzom Strassmannom a rakúskym fyzikom Lise Meitnerovou, ktoré viedlo k objavu jadrového štiepenia (1939) a spustenie uránu. prvej reťazovej reakcie s kontrolovaným štiepením talianskeho fyzika Enrica Fermiho (1942).
Jediným prirodzene sa vyskytujúcim izotopom je stabilný berýlium-9, hoci je známych 11 ďalších syntetických izotopov. Ich polčasy sa pohybujú od 1,5 milióna rokov (pre berylium-10, ktoré podlieha beta rozpadu) do 6,7 × 10 17 sekúnd pre berylium-8 (ktoré sa rozpadajú pomocou emisie dvoch protónov). Rozpad berylia 7 (53,2-dňový polčas) na Slnku je zdrojom pozorovaných solárnych neutrín.